 Wiki90
Wiki90
Wiki90: Enciclopedia stilului anilor 90 pe web

|

|

|

|




Cloroform
În acest articol, vom explora Cloroform din unghiuri diferite, cu scopul de a oferi o viziune cuprinzătoare și îmbogățitoare asupra acestui subiect. De la origine și până la relevanța sa astăzi, prin multiplele aplicații și domeniul de aplicare, ne vom cufunda într-o analiză profundă și detaliată care va permite cititorului să înțeleagă importanța și impactul Cloroform în diverse contexte. Prin dovezi științifice, mărturii ale experților și experiențe personale, vom face lumină asupra aspectelor necunoscute și fascinante ale Cloroform, contribuind astfel la înțelegerea și aprecierea acestui element fundamental în societatea noastră.
| Cloroform | |
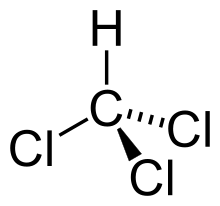 | |
| Nume IUPAC | Triclorometan |
|---|---|
| Alte denumiri | Cloroform Clorură de metin Clorură de metilidin |
| Identificare | |
| Număr CAS | 67-66-3 |
| ChEMBL | CHEMBL44618 |
| PubChem CID | 6212 |
| Informații generale | |
| Formulă chimică | CHCl3 |
| Aspect | lichid incolor |
| Masă molară | 119,38 g/mol |
| Proprietăți | |
| Densitate | 1,48 g/cm3 (20 °C) |
| Starea de agregare | lichidă |
| Punct de topire | −63 °C |
| Punct de fierbere | 61 °C |
| Solubilitate | bună în etanol, eter, benzol, aproape insolubil în apă |
| Presiune de vapori | 160 de millimetre of mercuryi |
| Fraze R | R22, R38, R40, R48/20/22 |
| Fraze S | (S2), S36/37 |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Cloroformul sau triclorometanul este o hidrocarbură clorurată cu formula chimică CHCl3. A fost descoperit în 1831 de Justus von Liebig, Samuel Guthrie și Eugène Soubeiran.
Proprietăți
Triclorometanul este un lichid incolor, neinflamabil cu un miros dulceag. Are o densitate mai mare decât apa, fiind solubil numai în solvenți organici. Vaporii de cloroform determină prin inhalare pierderea cunoștinței și reducerea sensibilității la durere. Din cauza efectului toxic asupra inimii, ficatului și altor organe interne, în prezent nu mai este folosit ca narcotic. Se presupune că ar avea și un efect cancerigen. Cloroformul în prezența oxigenului la lumină se descompune formându-se fosgen, clor și acid hipocloros (HClO). Cloroformul existent în comerț este un amestec cu 0,5–1,0 % etanol ca stabilizator.
Obținere
Pe scară industrială cloroformul se obține prin încălzirea la 400–500 °C a clorului cu metan sau clorură de metan, având loc o reacție de substituție:
In final rezultă un amestec de cloruri de metan care se separă printr-o distilare fracționată.
Utilizare
Cloroformul este folosit mai ales ca diluant și la producerea clorofluorocarburi care este răspunzător de formarea golurilor de ozon din straturile superioare ale atmosferei. Cloroformul deuterizat, (CDCl3), fiind numit cloroform-deuteriu este utilizat în spectroscopia nucleară (NMR).
Bioremedirea cloroformului
Unele bacterii anaerobe folosesc cloroformul pentru respirație, în procesul numit respirație organohalidă(en), convertindu-l în diclormetan.
Note
- ^ „cloroform”, CHLOROFORM (în engleză), PubChem, accesat în
- ^ http://www.cdc.gov/niosh/npg/npgd0127.html Lipsește sau este vid:
|title=(ajutor) - ^ Shuiquan Tang, Elizabeth A. Edwards (). „Identification of Dehalobacter reductive dehalogenases that catalyse dechlorination of chloroform, 1,1,1-trichloroethane and 1,1-dichloroethane”. Philos Trans R Soc Lond B Biol Sci. 368. doi:10.1098/rstb.2012.0318.
- ^ Jugder, Bat-Erdene; Ertan, Haluk; Wong, Yie Kuan; Braidy, Nady; Manefield, Michael; Marquis, Christopher P.; Lee, Matthew (). „Genomic, transcriptomic and proteomic analyses of Dehalobacter UNSWDHB in response to chloroform”. Environmental Microbiology Reports (în engleză). 8 (5): 814–824. doi:10.1111/1758-2229.12444. ISSN 1758-2229.
Legături externe
- Chloroform "The Molecular Lifesaver" An article at Oxford University providing facts about chloroform.
- Concise International Chemical Assessment Document 58
- IARC Summaries & Evaluations: Vol. 1 (1972), Vol. 20 (1979), Suppl. 7 (1987), Vol. 73 (1999)
- NIST Standard Reference Database
- Story on Chloroform from BBC's The Material World (28 July 2005)
- Sudden Sniffer's Death Syndrome Arhivat în , la Wayback Machine. article at Carolinas Poison Center
- Calculation of vapor pressure, liquid density, dynamic liquid viscosity, surface tension of chloroform
- ChemSub Online: Chloroform – Methane, trichloro-
 Chloroform
Chloroform Kloroform
Kloroform Chloroform
Chloroform Chloroform
Chloroform Cloroformo
Cloroformo Kloroformi
Kloroformi Chloroforme
Chloroforme Kloroform
Kloroform Cloroformio
Cloroformio Chloroform
Chloroform Chloroform
Chloroform Clorofórmio
Clorofórmio Kloroform
Kloroform Kloroform
Kloroform






